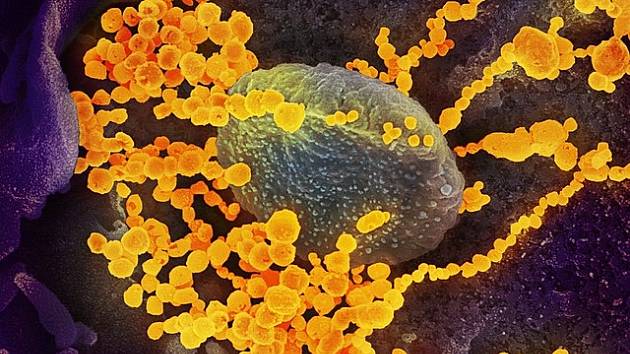
Gen LZTFL1 se podílí na tom, jak plicní buňky reagují na infekci virem SARS-CoV-2. Pokud se v lidském organismu vyskytuje ve své rizikové variantě, jsou tyto buňky vůči viru zřejmě zranitelnější. Ukazuje to nový výzkum vědců z Oxfordské univerzity.
Jeden z mnoha faktorů, ale důležitý
"Vysvětlit každý aspekt rizika takové nemoci, jako je covid-19, samozřejmě nelze jen jedním jednotlivým genem. Roli hraje spousta faktorů, jako je věk, celkový zdravotní stav i socioekonomická situace. To vše může ovlivnit jak to, jak moc je člověk viru vystaven, tak i to, jak kvalitní zdravotní péče se mu potom dostane," uvedl pro titul Live Science James Davies, profesor genomiky na Oxfordské univerzitě a jeden z vedoucích nového výzkumu.
"Například Indie zažila během nárůstu nákazy variantou Delta přetížené nemocnice a současně má tato země vysokou prevalenci srdečních chorob a diabetu 2. typu, což v úmrtnosti její populace sehrálo obrovskou roli. Nicméně gen LZTFL1 představuje jeden z nejrozšířenějších genetických signálů."
Podle autorů nové studie je u lidí ve věku mezi 20 a 60 lety v každé věkové skupině po deseti letech zhruba dvojnásobné riziko vážného průběhu, pokud daný člověk disponuje rizikovou variantou genu LZTFL1. "To znamená, že ho činí z hlediska nebezpečí závažnosti covid-19 zhruba o deset let staršího," uvedl Davies.
Vědci zkoumali zmíněný gen tzv. celogenomovou asociační studií, při níž porovnávali genomy skupiny pacientů s těžkým průběhem covid-19 (provázeným zápalem plic) s genomy kontrolní skupiny účastníků studie, kteří, ačkoli byli také nakaženi, netrpěli buď žádnými příznaky infekce, nebo jenom mírnými.
Dálkový genový ovladač
Studie ukázala, že u vážně postižených pacientů se častěji vyskytovala určitá sada genů, ale bylo těžké zjistit, který z nich skutečně zvyšuje riziko vážného průběhu.
"Genové variace se často dědí jako celý balíček, takže určit, za co která konkrétní verze konkrétně zodpovídá, je docela složité," říká Jim Hughes, profesor genové regulace na Oxfordské univerzitě a jeden ze spoluatorů studie. Byť jsou totiž genetické sekvence přítomny v každé buňce těla, ovlivňují pouze několik typů buněk.

Navíc genetické sekvence, které vědci zkoumali, představovaly velmi složité "vylepšovací" a "zesilovací" sekvence, fungující trochu jako dálkový ovladač či zesilovač: "zapínaly" a "vypínaly" geny v různém čase a v různých tkáních, a přitom se často nemusely ani zdaleka nacházet v jejich blízkosti.
Aby tento problém vyřešili, využili vědci strojového učení a chtěli po něm, aby na základě sekvence DNA předpovědělo, jaký typ buněk bude tento ovladač či zesilovač ovlivňovat. "Umělá inteligence pak rozsvítila jeden konkrétní zesilovač jako vánoční stromeček," uvedl Hughes.
Vědci podle serveru Science Alert původně očekávali, že nejrizikovější vylepšovací sekvencí bude taková, která působí na geny imunitního systému. Fakt, že místo toho "řádí" v plicních buňkách, je překvapil.
Dalším krokem bylo zjistit, jaký gen je tímto ovladačem kontrolován. Za tímto účelem použili vědci techniku zvanou Micro Capture-C, která umožňuje extrémně podrobné mapování spleti DNA uvnitř buněčného jádra. Zjistili, že zesilovač působil pouze na jeden gen: LZTFL1.
Podle Hughese je genový vliv na závažnost onemocnění covid-19 v porovnání s tím, co tato technika ukazuje při genovém ovlivnění jiných nemocí jako třeba ischemická choroba srdeční nebo cukrovka či cokoli jiného, opravdu masivní. "Je to neuvěřitelně silné," uvedl Hughes.
Výzkum může změnit léčbu
LZTFL1 nebyl dosud příliš zkoumán, přesto však vědci již dříve zjistili něco o bílkovině, kterou kóduje a která se podílí na signalizaci ran a na jejich následném hojení. Trpí-li lidské tělo zánětem a infekcí, pak nízká hladina LZTFL1 podporuje přechod určitých specializovaných plicních buněk do méně specializovaného stavu, zatímco vyšší hladina LZTFL1 tento přechod brzdí.
U pacientů s těžkým průběhem covid-19 k tomuto přechodu zcela jistě dochází. Výzkumný tým studoval biopsie těch lidí, kteří na nákazu covid-19 zemřeli, a zjistil, že jejich plíce pokryly velké plochy právě těchto despecializovaných buněk. Může jít ale právě o to, že plíce se snaží se tímto způsobem chránit.
"Ještě to není jisté, ale zdá se, že despecializované plicní buňky mají méně receptorů ACE2, což jsou dveře, jimiž si SARS-CoV-2 otevírá cestu do buněk. Mohou tak být před virem lépe chráněny. Vysoká hladina LZTFL1 ale přechod buněk do této obranné pozice zpomaluje, což viru umožňuje, aby mezitím pustošil plíce," uvádí Davies. Podle něj však musí tuto teorii ještě potvrdit přímý výzkum poškození plic covidem, než bude možné považovat ji za prokázanou.
Podle Hughese může objev významu LZTFL1, o němž jako první informoval 4. listopadu časopis Nature Genetics, vést k novým způsobům léčby covid-19. Nabízí se například možnost přednostně nabízet očkování nejzranitelnějším etnikům, třeba právě osobám jihoasijského původu. Protože zmíněný gen není zapojen do imunitního systému, je pravděpodobné, že i nositelé jeho vysoce rizikové verze zareagují na očkování stejně jako všichni ostatní, a riziko vážného průběhu se u nich sníží.